Nat Med | Fjölþátta nálgun til að kortleggja samþætt æxlis-, ónæmis- og örverufræðilegt landslag ristilkrabbameins leiðir í ljós samspil örveruflórunnar við ónæmiskerfið.
Þótt lífmerki fyrir frumkomið ristilkrabbamein hafi verið rannsökuð ítarlega á undanförnum árum, byggja núverandi klínískar leiðbeiningar eingöngu á stigun æxlis í eitlum og meinvörpum og greiningu á DNA misræmisviðgerð (MMR) eða öróstöðugleika (MSI) (auk hefðbundinna meinafræðiprófa) til að ákvarða meðferðarráðleggingar. Rannsakendur hafa tekið eftir skorti á tengslum milli ónæmissvörunar sem byggjast á genatjáningu, örverusniðum og æxlisstroma í ristilkrabbameinshópnum Cancer Genome Atlas (TCGA) og lifun sjúklinga.
Eftir því sem rannsóknir hafa þróast hefur verið greint frá því að megindleg einkenni frumkrabbameins í ristli og endaþarmi, þar á meðal frumu-, ónæmis-, bandvefs- eða örverufræðilegs eðlis krabbameinsins, hafi marktækan fylgni við klínískar niðurstöður, en enn er takmörkuð skilningur á því hvernig samspil þeirra hefur áhrif á niðurstöður sjúklinga.
Til að greina tengslin milli flækjustigs svipgerðar og útkomu þróaði teymi vísindamanna frá Sidra Institute of Medical Research í Katar nýlega og staðfesti samþættan stigatöflu (mICRoScore) sem greinir hóp sjúklinga með góða lifunartíðni með því að sameina einkenni örveruflórunnar og ónæmishöfnunarstuðla (ICR). Teymið framkvæmdi ítarlega erfðagreiningu á ferskum frystum sýnum frá 348 sjúklingum með krabbamein í ristli og endaþarmi, þar á meðal RNA raðgreiningu æxla og paraðs heilbrigðs ristilvefs, heildar exome raðgreiningu, djúpa T-frumuviðtaka og 16S bakteríu rRNA gena raðgreiningu, ásamt heildarerfðamengisraðgreiningu æxla til að lýsa örveruflórunni frekar. Rannsóknin var birt í Nature Medicine sem „Samþætt æxlis-, ónæmis- og örveruflórukrabbameinsatlas“.

Grein birt í Nature Medicine
Yfirlit yfir AC-ICAM
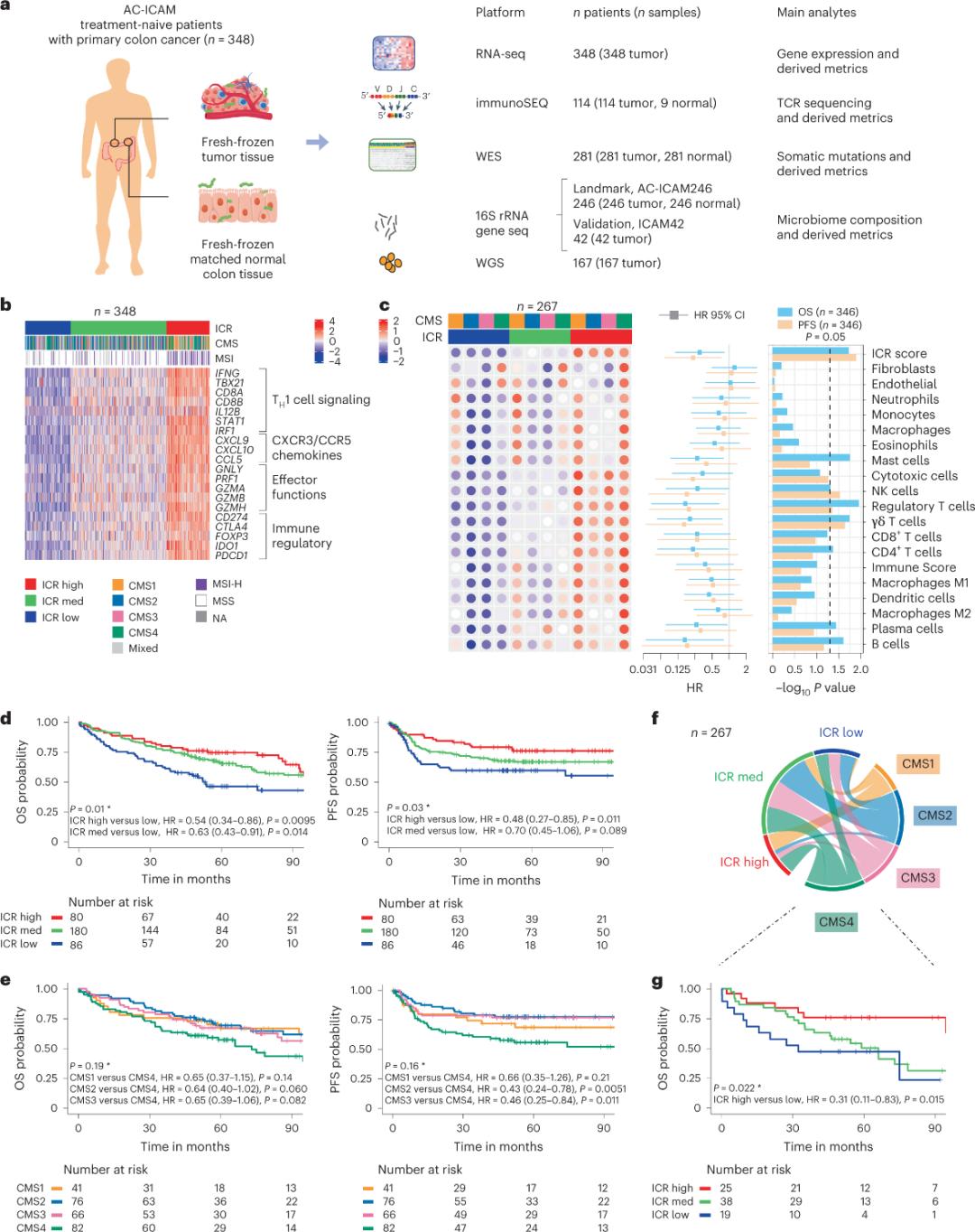
Rannsakendur notuðu rétthyrndan erfðafræðilegan vettvang til að greina fersk frosin æxlissýni og para saman aðliggjandi heilbrigðan ristilvef (æxlis-eðlileg pör) frá sjúklingum með vefjagreiningu á ristilkrabbameini án kerfisbundinnar meðferðar. Byggt á heildar exome raðgreiningu (WES), gæðaeftirliti með RNA-raðgreiningargögnum og skimun samkvæmt aðkomuviðmiðum voru erfðafræðileg gögn frá 348 sjúklingum geymd og notuð til síðari greiningar með miðgildi eftirfylgnitíma 4,6 ár. Rannsóknarhópurinn nefndi þessa auðlind Sidra-LUMC AC-ICAM: Kort og leiðbeiningar um ónæmis-krabbameins-örveruflóru milliverkanir (Mynd 1).
Sameindaflokkun með ICR
Rannsóknarteymið safnaði saman einingum af erfðafræðilegum merkjum ónæmiskerfisins fyrir stöðuga krabbameinsónæmiseftirlit, kallað ónæmisstuðullinn fyrir höfnun (ICR), og fínstillti ICR með því að þjappa honum niður í 20 gena spjald sem nær yfir mismunandi tegundir krabbameins, þar á meðal sortuæxli, þvagblöðrukrabbamein og brjóstakrabbamein. ICR hefur einnig verið tengt við ónæmismeðferðarsvörun í ýmsum tegundum krabbameins, þar á meðal brjóstakrabbameini.
Fyrst staðfestu vísindamennirnir ICR-einkenni AC-ICAM hópsins með því að nota ICR-genatengda samflokkunaraðferð til að flokka hópinn í þrjá klasa/ónæmisgerðir: hátt ICR (heit æxli), miðlungs ICR og lágt ICR (köld æxli) (Mynd 1b). Rannsakendur greindust ónæmisónæmisbreytingum sem tengdust samhljóða sameindagerðum (CMS), sem er umritunarbundin flokkun ristilkrabbameins. CMS-flokkarnir innihéldu CMS1/ónæmi, CMS2/viðurkennt, CMS3/efnaskipta og CMS4/mesenchymalt. Greiningin sýndi að ICR-stig voru neikvæð fylgni við ákveðnar krabbameinsfrumuferla í öllum CMS-undirgerðum og jákvæð fylgni við ónæmisbælandi og bandvefstengda ferla sást aðeins í CMS4 æxlum.
Í öllum CMS var fjöldi náttúrulegra drápsfrumna (NK-frumna) og T-frumna mestur í undirflokkum ICR með hátt ónæmiskerfi, með meiri breytileika í öðrum undirflokkum hvítfrumna (mynd 1c). Undirflokkar ICR ónæmiskerfisins höfðu mismunandi heildarlifun (OS) og lifun án framvindu sjúkdóms (PFS), með stigvaxandi aukningu á ICR frá lágu til háu (mynd 1d), sem staðfestir spádómshlutverk ICR í ristilkrabbameini.
Mynd 1. Hönnun AC-ICAM rannsóknarinnar, ónæmistengd genasería, ónæmis- og sameindaundirgerðir og lifun.
ICR fangar æxlisríkar, klónalega magnaðar T-frumur
Aðeins minnihluti T-frumna sem síast inn í æxlisvef hefur reynst sértækir fyrir æxlisvaka (minna en 10%). Þess vegna eru meirihluti innanæxlis-T-frumna nefndir bystander T-frumur (bystander T-frumur). Sterkasta fylgnin við fjölda hefðbundinna T-frumna með afkastamiklar TCR-frumur sást í bandvefsfrumum og hvítfrumnum (greind með RNA-seq), sem hægt er að nota til að meta T-frumuundirhópa (Mynd 2a). Í ICR-klösum (heildar- og CMS-flokkun) sást hæsta klónun ónæmis-SEQ TCR-frumna í ICR-háu og CMS undirgerð CMS1/ónæmishópunum (Mynd 2c), með hæsta hlutfalli ICR-háu æxla. Með því að nota allt umritið (18.270 gen) voru sex ICR-gen (IFNG, STAT1, IRF1, CCL5, GZMA og CXCL10) meðal tíu efstu gena sem tengdust jákvætt TCR ónæmis-SEQ klónun (Mynd 2d). Klónleiki ImmunoSEQ TCR fylgnist sterkar flestum ICR genum en fylgnin sem sést með æxlisbreyttum CD8+ merkjum (Mynd 2f og 2g). Að lokum bendir ofangreind greining til þess að ICR undirskriftin fangi nærveru æxlisauðgaðra, klónalega magnaðra T frumna og gæti skýrt spádómsáhrif hennar.
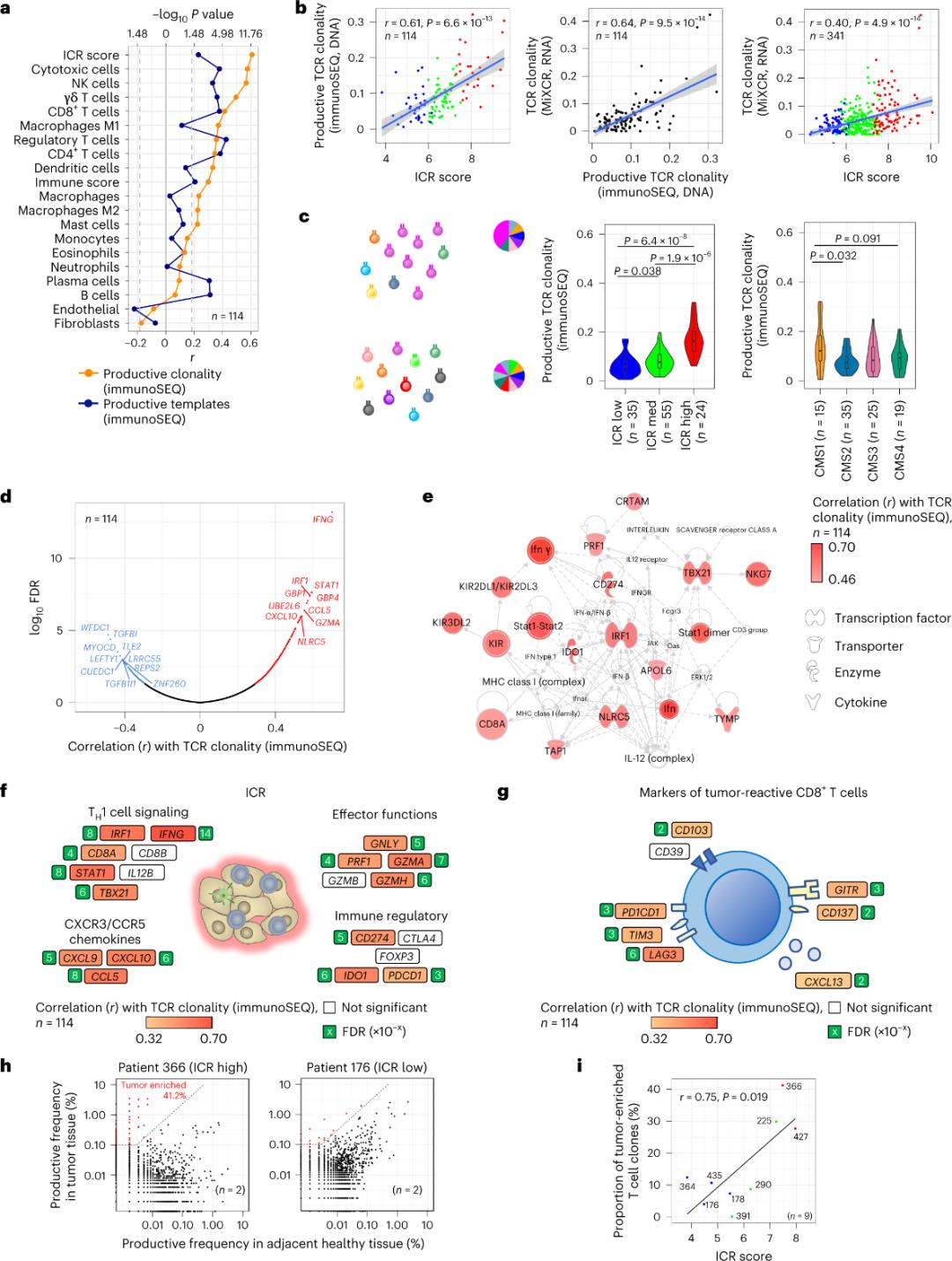
Mynd 2. TCR mælikvarðar og fylgni við ónæmistengd gen, ónæmis- og sameindaundirgerðir.
Samsetning örveruflóru í heilbrigðum vefjum og krabbameinsvefjum í ristli
Rannsakendurnir framkvæmdu 16S rRNA raðgreiningu með því að nota DNA sem unnið var úr samsvarandi æxlisvef og heilbrigðum ristilvef frá 246 sjúklingum (Mynd 3a). Til staðfestingar greindu rannsakendurnir einnig gögn um 16S rRNA genaröðun úr 42 viðbótaræxlissýnum sem höfðu ekki samsvarandi eðlilegt DNA tiltækt til greiningar. Fyrst báru rannsakendurnir saman hlutfallslegan fjölda flóru milli samsvarandi æxla og heilbrigðs ristilvefs. Clostridium perfringens var marktækt aukinn í æxlunum samanborið við heilbrigð sýni (Mynd 3a-3d). Enginn marktækur munur var á alfa fjölbreytileika (fjölbreytileika og fjölda tegunda í einu sýni) milli æxlis- og heilbrigðra sýna, og lítilsháttar minnkun á örverufjölbreytileika sást í æxlum með hátt ICR samanborið við æxli með lágt ICR.
Til að greina klínískt mikilvæg tengsl milli örverusniða og klínískra útkoma, stefndu vísindamennirnir að því að nota gögn úr raðgreiningu 16S rRNA gena til að bera kennsl á eiginleika örveruflórunnar sem spá fyrir um lifun. Í AC-ICAM246 keyrðu vísindamennirnir OS Cox aðhvarfslíkan sem valdi 41 eiginleika með stuðlum sem eru ekki núll (tengdir mismunandi dánartíðniáhættu), kallaðir MBR flokkarar (Mynd 3f).
Í þessum þjálfunarhópi (ICAM246) tengdist lágt MBR-stig (MBR<0, lágt MBR) marktækt minni dánarhættu (85%). Rannsakendur staðfestu tengslin milli lágs MBR (áhættu) og lengdrar heildarlifunar í tveimur sjálfstætt staðfestum hópum (ICAM42 og TCGA-COAD). (Mynd 3) Rannsóknin sýndi sterka fylgni milli innmagakokka og MBR-stiga, sem voru svipuð í æxlisvef og heilbrigðum ristilvef.
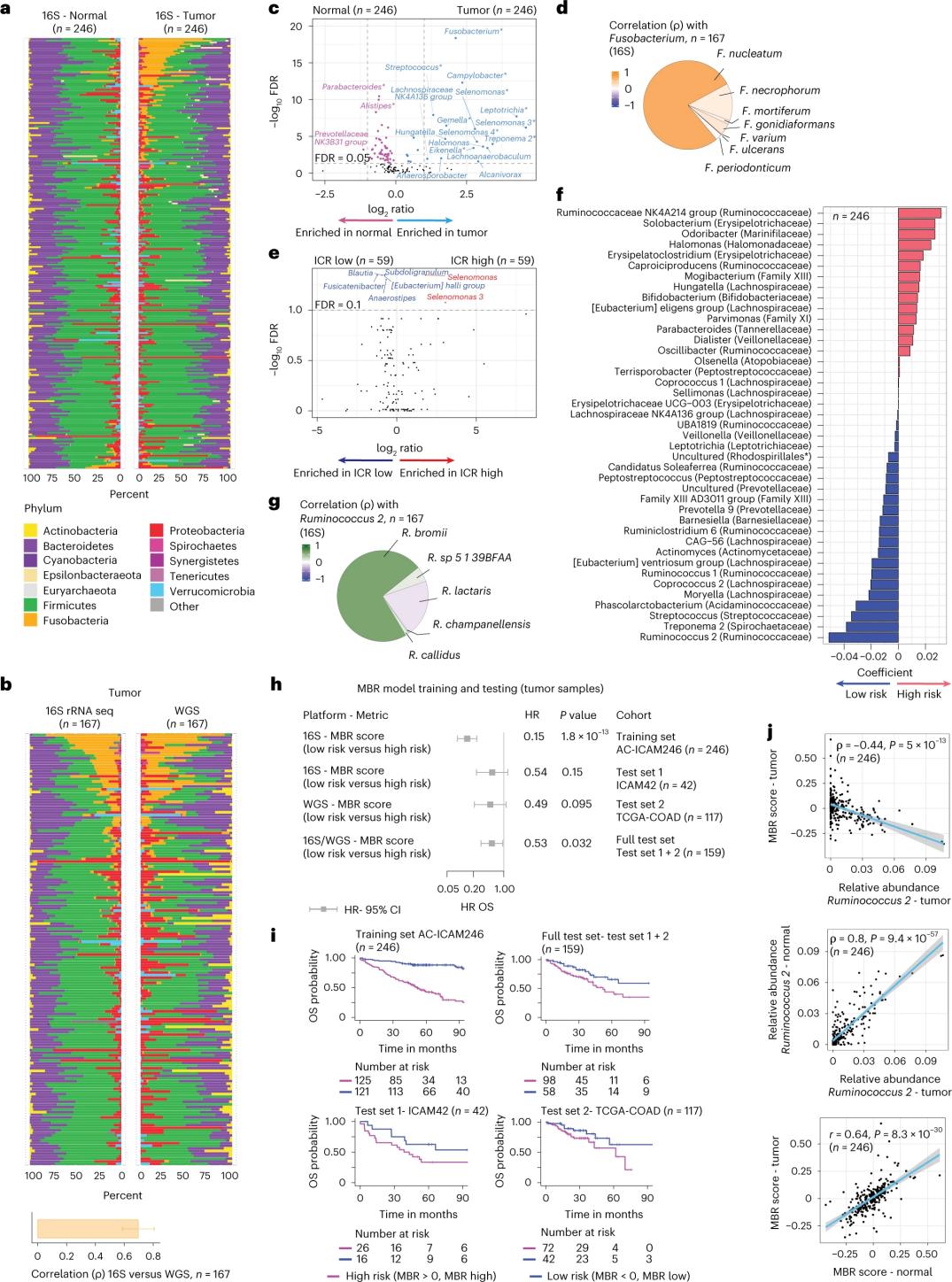
Mynd 3. Örveruflóra í æxli og heilbrigðum vefjum og tengsl þess við ICR og lifun sjúklinga.
Niðurstaða
Fjölþátta nálgunin sem notuð var í þessari rannsókn gerir kleift að greina og greina sameindaeiginleika ónæmissvörunar í ristilkrabbameini í endaþarmi ítarlega og leiðir í ljós samspil örveruflórunnar og ónæmiskerfisins. Djúp TCR raðgreining á æxli og heilbrigðum vefjum leiddi í ljós að spádómsáhrif ICR gætu stafað af getu þess til að fanga æxlisauðgaða og hugsanlega æxlismótefnavaka-sértæka T-frumuklóna.
Með því að greina samsetningu æxlisörveruflórunnar með því að nota 16S rRNA genaröðun í AC-ICAM sýnum, greindi teymið einkenni örveruflórunnar (MBR áhættustig) með sterkt spágildi. Þó að þessi einkenni væru fengin úr æxlissýnum, var sterk fylgni milli heilbrigðs ristil- og endaþarms og MBR áhættustigs æxlis, sem bendir til þess að þessi einkenni gætu fangað samsetningu þarmaörveruflórunnar hjá sjúklingum. Með því að sameina ICR og MBR stig var hægt að bera kennsl á og staðfesta fjölþátta nemendalífmerki sem spáir fyrir um lifun hjá sjúklingum með ristilkrabbamein. Fjölþátta gagnasafn rannsóknarinnar veitir úrræði til að skilja betur líffræði ristilkrabbameins og hjálpa til við að uppgötva sérsniðnar meðferðaraðferðir.
Birtingartími: 15. júní 2023
 中文网站
中文网站